Betegtájékoztató: Információk a felhasználó számára
Berinert 2000 NE por és oldószer oldatos injekcióhoz
humán C1-észteráz-inhibitor
Mielőtt elkezdi alkalmazni ezt a gyógyszert, olvassa el figyelmesen az alábbi betegtájékoztatót, mert az Ön számára fontos információkat tartalmaz.
- Tartsa meg a betegtájékoztatót, mert a benne szereplő információkra a későbbiekben is szüksége lehet.
- További kérdéseivel forduljon kezelőorvosához vagy gyógyszerészéhez.
- Ezt a gyógyszert az orvos kizárólag Önnek írta fel. Ne adja át a készítményt másnak, mert számára ártalmas lehet még abban az esetben is, ha a betegsége tünetei az Önéhez hasonlóak.
- Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. Lásd 4. pont
A betegtájékoztató tartalma:
- Milyen típusú gyógyszer a Berinert 2000 NE injekció és milyen betegségek esetén alkalmazható?
- Tudnivalók a Berinert 2000 NE injekció alkalmazása előtt
- Hogyan kell alkalmazni a Berinert 2000 NE injekciót?
- Lehetséges mellékhatások
- Hogyan kell a Berinert 2000 NE injekciót tárolni?
- További információk
- Milyen típusú gyógyszer a Berinert 2000 NE injekció és milyen betegségek esetén alkalmazható?
Mi a Berinert 2000 NE injekció?
A Berinert 2000 NE (Nemzetközi Egység) injekció por és oldószer. A kész oldat injekcióként bőr alá adandó.
A Berinert 2000 NE injekciót emberi plazmából (a vér folyékony része) állítják elő, aktív hatóanyaga az emberi (humán) C1–észteráz‑inhibitor fehérje.
Mire alkalmazható a Berinert 2000 NE injekció?
A Berinert 2000 NE injekciót ismétlődő örökletes (herediter) angioödéma (HAE, ödéma = vizenyős duzzanat) rohamok megelőzésére alkalmazzák C1-észteráz inhibitor hiányában szenvedő serdülő és felnőtt betegeknél.
A herediter angioödéma (HAE) az érrendszer örökletes betegsége. Nem allergiás eredetű. A HAE oka a C1‑észteráz–inhibitor fehérje kialakulásának elégtelensége, hiánya, vagy károsodása. A betegség az alábbi tünetekkel jellemezhető:
– a kezeken és a lábakon hirtelen kialakuló vizenyős duzzanat,
– az arcon hirtelen kialakuló vizenyős duzzanat feszülő érzéssel,
– szemhéj-, ajakduzzanat, lehetséges gégevizenyő, ami nehézlégzést okoz,
– nyelvduzzanat,
– görcsös fájdalom a has területén.
Általában a test minden részén kialakulhat.
- Tudnivalók a Berinert 2000 NE injekció alkalmazása előtt
Az ebben a részben szereplő információkat az Ön kezelőorvosának figyelembe kell vennie, mielőtt Ön Berinert 2000 NE injekciót kapna.
Ne alkalmazza a Berinert 2000 NE injekciót
- ha életet veszélyeztető azonnali túlérzékenységi reakciók alakultak ki Önnél, beleértve a C1‑észteráz-inhibitor fehérjével vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjével szembeni anafilaxiás reakciót.
Kérjük, tájékoztassa kezelőorvosát vagy gyógyszerészét bármilyen gyógyszer- vagy élelmiszerallergiájáról.
Figyelmeztetések és óvintézkedések
A Berinert alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével:
- ha súlyos allergiás vagy anafilaxiás típusú reakciók alakulnak ki Önnél (utóbbi olyan súlyos allergiás reakció, amely komoly légzési nehézséget vagy szédülést vált ki). Azonnal fel kell függeszteni a Berinert alkalmazását (vagyis meg kell szakítani az injekció beadását).
- ha korelőzményében véralvadási zavarai szerepeltek. Az intravénás Berinerttel kezelt betegeknél előfordultak vérrögképződések. Ha a Berinertet nagyon magas dózisban adják a HAE-től eltérő betegségek kezelésére, megnőhet a vérrögök kialakulásának kockázata. Mindazonáltal a bőr alá adott Berinert esetében nincs egyértelmű kapcsolat a vérrögök kialakulásával a kezelőorvosa általi felírásra ajánlott dózisok esetében. Szóljon kezelőorvosának, ha a kórtörténetében előfordult szív- vagy érbetegség, agyvérzés, vérrögök kialakulása, vagy ha magas a trombocita száma, állandó katéter vagy hozzáférési eszköz van valamelyik vénájába ültetve, vagy ha egy ideje ágyhoz kötött állapotban van. Ezek ugyanis fokozhatják a vérrögök kialakulásának kockázatát Berinert alkalmazását követően. Továbbá tájékoztassa kezelőorvosát a jelenleg alkalmazott gyógyszereiről, ugyanis egyes gyógyszerek – például a születésszabályozásra használt tabletták vagy egyes férfi nemi hormonok – fokozhatják a vérrög kialakulásának kockázatát.
Az Ön kezelőorvosa gondosan mérlegelni fogja a Berinert‑kezelés előnyeit, összehasonlítva a lehetséges komplikációk kockázatával.
Vírusbiztonság
Az emberi vérből vagy plazmából előállított készítmények gyártásánál szigorú rendszabályokat alkalmaznak, hogy a fertőzések átvitelét megakadályozzák. Ezek az alábbiak:
- A vért, illetve plazmát adó donorok gondos kiválasztása, amivel kizárják a fertőzés átvitelének kockázatát, és
- minden egyes plazmaadományt és plazmakeveréket ellenőriznek vírusok, illetve egyéb fertőző ágensek jelenlétére.
A gyártók a vér vagy plazma feldolgozási folyamatában vírusinaktiváló vagy víruseltávolító lépéseket alkalmaznak. Ennek ellenére az emberi vérből vagy plazmából előállított gyógyszerek alkalmazása esetén nem zárható ki teljesen fertőző ágensek átvitele. Ez vonatkozik ismeretlen vagy újonnan felbukkanó vírusokra és egyéb típusú fertőzésekre is.
Az alkalmazott módszerek hatékonyak a burokkal rendelkező vírusoknál, például humán immundeficiencia vírus (HIV, az AIDS vírusa), hepatitisz B‑vírus és hepatitisz C‑vírus (májgyulladás) és a burokkal nem rendelkező vírusoknál, mint a hepatitisz A vírus (májgyulladás) és a parvovírus B19.
Amennyiben Ön rendszeresen vagy ismétlődően kap emberi plazmából előállított termékeket, kezelőorvosa azt javasolhatja Önnek, hogy fontolja meg a hepatitisz A és B elleni védőoltás beadatását.
Kifejezetten javasolt, hogy minden alkalommal, amikor a Berinert beadásra kerül, fel kell jegyezni a beadás dátumát, a készítmény gyártási számát és a beadott injekció térfogatát.
Egyéb gyógyszerek és a Berinert
- Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben alkalmazott, valamint alkalmazni tervezett egyéb gyógyszereiről. Ez vonatkozik a recept nélkül kapható készítményekre is.
- Berinert nem keverhető egyéb gyógyszerrel és oldószerrel a fecskendőben.
Terhesség és szoptatás
Amennyiben Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A Berinert nem befolyásolja a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
A Berinert 2000 NE injekció nátriumot tartalmaz
Ez a gyógyszer kevesebb, mint 1 mmol (23 mg) nátriumot tartalmaz injekciós üvegenként, azaz gyakorlatilag „nátriummentes”.
- Hogyan kell alkalmazni a Berinert 2000 NE injekciót?
A Berinert önbeadásra, bőr alatti injekcióban történő alkalmazásra javasolt. Szükség esetén Önnek vagy gondozójának meg kell tanulnia, hogyan kell beadnia a Berinertet.
Adagolás
A Berinert javasolt adagja 60 NE testtömeg-kilogrammonként.
Gyermekek és serdülők
A javasolt adagolás ugyanaz, mint a felnőtteknél.
Ha az előírtnál több Berinert 2000 NE injekciót alkalmazott
Túladagolásról szóló esetet nem jelentettek.
Feloldás és az alkalmazás módja
Ha az Ön kezelőorvosa úgy találja, hogy Ön alkalmas lehet az otthoni kezelésre, részletes oktatást fog Önnek tartani. Önnek egy naplót kell vezetnie, amelyben az otthoni kezelést dokumentálja, és ezt a naplót minden esetben magával kell vinnie kezelőorvosához. Ön vagy a gondozója beadási technikáját rendszeresen ellenőrizni fogják, ami biztosítja a folyamatos, megfelelő kezelést.
Általános utasítás
- A por feloldását és az oldat felszívását az injekciós üvegből aszeptikus körülmények között kell elvégezni. Alkalmazza a termékhez mellékelt fecskendőt.
- Az elkészített oldat színtelen, és tiszta vagy enyhén opálos. Szűrés vagy a felszívás után (lásd alább), beadás előtt az oldatot megtekintéssel ellenőrizni kell színváltozásra és apró részecskék jelenlétére.
- Ne használja az oldatot, ha láthatóan zavaros vagy pelyheket, részecskéket tartalmaz.
- A fel nem használt készítmény, illetve hulladékanyag megsemmisítését a helyi előírások szerint és az Ön kezelőorvosának instrukcióinak megfelelően kell végrehajtani.
Visszaoldás
A Berinert port és oldószert tartalmazó üvegeit bontatlanul melegítse szobahőmérsékletre. Ezt megteheti úgy, hogy az üvegeket szobahőmérsékletre helyezi kb. 1 órára, vagy néhány percig a kezében tartja. Ne melegítse közvetlenül az üvegeket. Az üvegeket nem szabad testhőmérséklet (37°C) fölé melegíteni.
A készítményt és az oldószert tartalmazó injekciós üvegek védőkupakját óvatosan távolítsa el. Mindkét injekciós üveg gumidugóját tisztítsa meg egy-egy alkoholos törlővel, és hagyja megszáradni. Az oldószer most már áttölthető a port tartalmazó üvegbe a mellékelt áttöltő készlet (Mix2Vial) segítségével. Kövesse az alábbi utasítást.
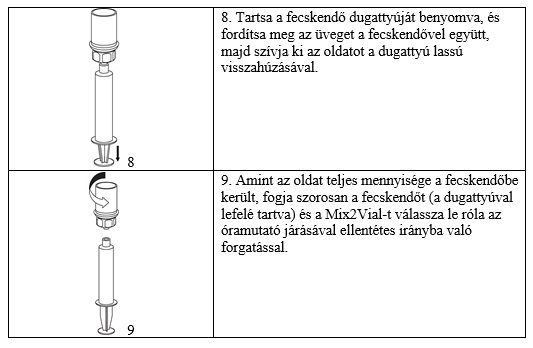
Felszívás és alkalmazás
- táblázat: Utasítások a Berinert önbeadásához
- Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Kérjük, haladéktalanul vegye fel a kapcsolatot kezelőorvosával:
- ha bármely mellékhatás előfordul, vagy
- ha Ön olyan mellékhatásokat észlel, ami nem szerepel ebben a betegtájékoztatóban.
A Berinerthez köthető nemkívánatos hatások ritkák.
A következő mellékhatásokat figyelték meg nagyon gyakran (vagyis 10 ember közül több mint 1 főt érinthetnek):
- Helyi reakciók az injekció beadási helyén (véraláfutás, hidegérzet, váladékozás, bőrpír, vérömleny, vérzés, keményedés, ödéma, fájdalom, viszketés, bőrkiütés, hegesedés, duzzanat, csalánkiütés, melegérzet).
- Orrgaratgyulladás (orrfolyás vagy orrdugulás, tüsszögés, könnyezés).
A következő mellékhatásokat figyelték meg gyakran (vagyis 10 ember közül legfeljebb 1 főt érinthetnek):
- Túlérzékenységi vagy allergiás reakciók (például túlérzékenység, viszketés, kiütés és csalánkiütés).
- Szédülés
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az V. függelékben található elérhetőségeken keresztül. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
- Hogyan kell a Berinert 2000 NE injekciót tárolni?
- A gyógyszer gyermekektől elzárva tartandó!
- A címkén és a dobozon feltüntetett lejárati idő (Felhasználható:) után ne alkalmazza ezt a gyógyszert.
- Legfeljebb 30 °C-on tárolandó.
- Nem fagyasztható!
- A fénytől való védelem érdekében az injekciós üvegek a külső csomagolásban tárolandók.
- A Berinert nem tartalmaz konzerváló szert, ezért feloldás után azonnal fel kell használni.
- Amennyiben az elkészített oldatot nem adják be azonnal, 8 órán belül szabad felhasználni és csak az injekciós üvegben szabad tárolni.
- A csomagolás tartalma és egyéb információk
Mit tartalmaz a Berinert 2000 NE injekció?
A készítmény hatóanyaga:
Emberi C1-észteráz-inhibitor (2000 NE/injekciós üveg; 4ml injekciós vízzel való feloldás után 500 NE/ml)
További információkért lásd a „Az alábbi információk kizárólag egészségügyi szakembereknek szólnak” fejezetet.
Egyéb összetevők:
Glicin, nátrium-klorid, nátrium-citrát.
Oldószer: injekcióhoz való víz.
Milyen a Berinert 2000 NE-et tartalmazó injekció külleme és mit tartalmaz a csomagolás?
A Berinert 2000 NE-et tartalmazó fehér port és az oldáshoz szükséges injekcióhoz való vizet tartalmaz. Az elkészített oldat színtelen és tiszta vagy enyhén opálos.
Kiszerelés
1 csomag Berinert 2000 NE por és oldószer oldatos injekcióhoz tartalma:
1 db port tartalmazó injekciós üveg
1 db injekciós üveg 4 ml injekcióhoz való vízzel
1 db szűrővel ellátott áttöltő eszköz 20/20
Beadáshoz szükséges készlet (egy belső dobozban)1 db 5 ml-es egyszer használatos fecskendő
1 db injekciós tű
1 db szubkután injekciós készlet
2 db alkoholos törlő
1 sebtapasz
Gyűjtőcsomag: 5×2000NE, 5 db Beadáshoz szükséges készlet (egy dobozban)
Gyűjtőcsomag: 20×2000NE, 4×5 db Beadáshoz szükséges készlet (négy dobozban)
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
A forgalomba hozatali engedély jogosultja és a gyártó
CSL Behring GmbH
Emil-von-Behring-Str. 76
35041 Marburg
Németország
Ezt a gyógyszert az Európai Gazdasági Térség tagállamaiban az alábbi neveken engedélyezték:
| Gyógyszer neve | Ország |
| Berinert 2000 IE Pulver und Lösungsmittel zur Herstellung einer Injektionslösung | Ausztria |
| Berinert 2000 IE, poeder en oplosmiddel
voor oplossing voor injectie |
Belgium |
| Berinert 2000 | Ciprus, Németország, Görögország, Lengyelország, Portugália |
| Беринерт 2000, Прах и разтворител
за инжекционен разтвор C1- естеразен инхибитор, човешки |
Bulgária |
| Berinert | Dánia, Olaszország, |
| Berinert 2000 IU, injektio/infuusiokuiva-aine
ja liuotin, liuosta varten |
Finnország |
| Berinert 2000 IU | Csehország, Szlovákia, |
| Berinert 2000 IU, poudre et solvant pour solution injectale | Franciaország, Luxemburg |
| Berinert 2000 NE por és oldószer oldatos injekcióhoz | Magyarország |
| Berinert 2000 IU pulver og væske til
injeksjonsvæske, oppløsning |
Norvégia |
| Berinert 2000 2000 UI, pulbere şi solvent pentru soluţie injectabilă | Románia |
| Berinert 2000 i.e. prašek in vehikel za
raztopino za injiciranje |
Szlovénia |
| Berinert 2000 UI polvo y disolvente
para solución inyectable subcutánea |
Spanyolország, |
| Berinert 2000 IE, pulver och vätska till
injektionsvätska, lösning |
Svédország |
| Berinert 2000 IU powder and solvent for solution for injection | Egyesült Királyság, Málta |
OGYI-T-5953/03 1× Port tartalmazó injekciós üveg (II-es típus) +
Oldószert tartalmazó injekciós üveg (I-es típus) +
1 db szűrővel ellátott áttöltő eszköz 20/20 +
az alkalmazáshoz szükséges felszerelés
OGYI-T-5953/04 5× Port tartalmazó injekciós üveg (II-es típus) +
Oldószert tartalmazó injekciós üveg (I-es típus) +
1 db szűrővel ellátott áttöltő eszköz 20/20 +
az alkalmazáshoz szükséges felszerelés
OGYI-T-5953/05 20× Port tartalmazó injekciós üveg (II-es típus) +
Oldószert tartalmazó injekciós üveg (I-es típus) +
1 db szűrővel ellátott áttöltő eszköz 20/20 +
az alkalmazáshoz szükséges felszerelés
A betegtájékoztató legutóbbi felülvizsgálatának dátuma: 2020. november